标题: 精准锁定免疫治疗耐药元凶!空间单细胞蛋白分型揭示NSCLC关键耐药细胞亚群
核心临床价值:
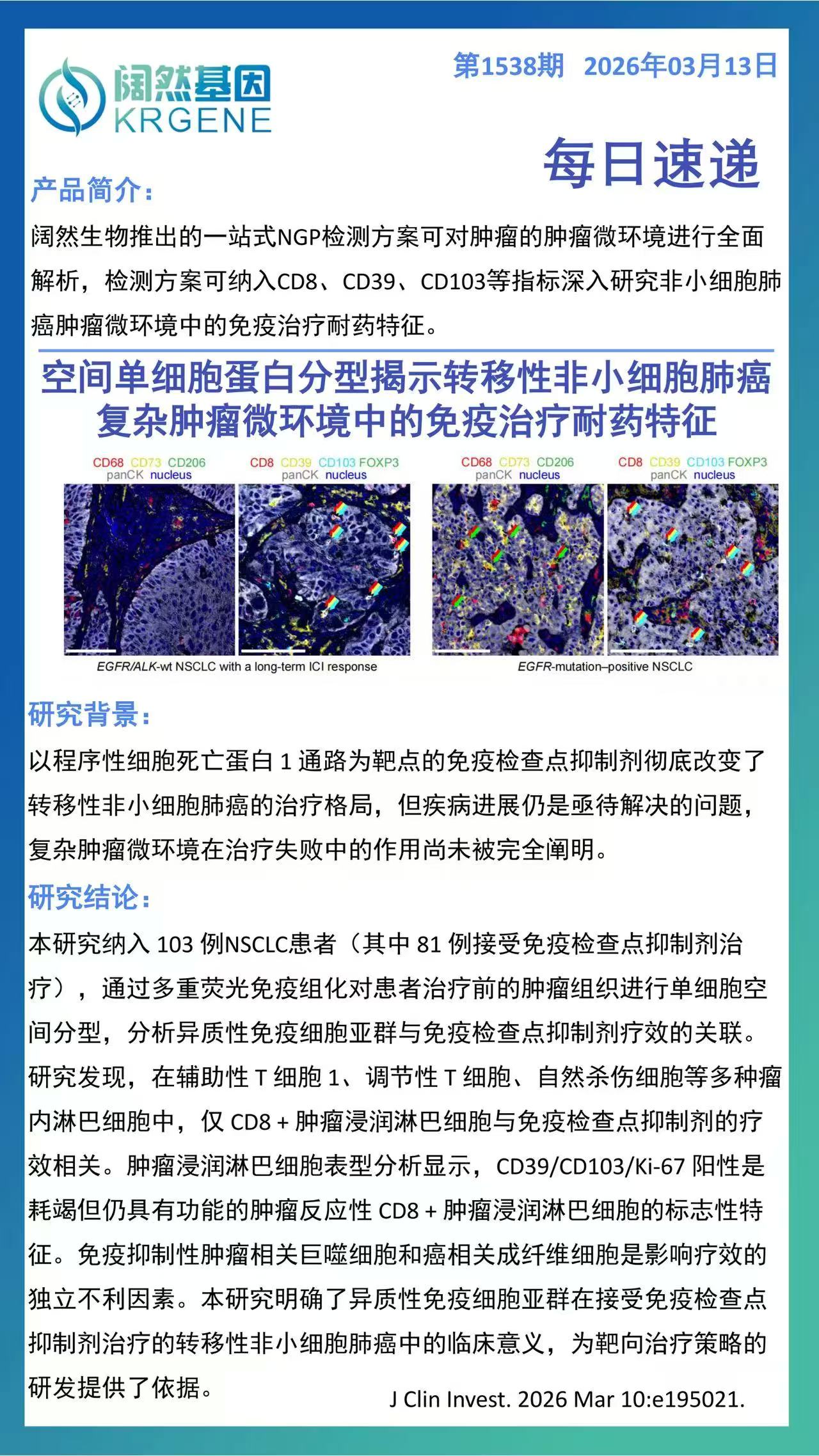
鉴定关键疗效预测性T细胞亚群:研究明确了在众多淋巴细胞中,唯有CD8+肿瘤浸润淋巴细胞(TILs) 与免疫检查点抑制剂(ICI)疗效直接相关。更重要的是,鉴定出CD39+CD103+Ki-67+ 三阳性CD8+ TILs是“耗竭但仍有功能”的肿瘤反应性T细胞的关键标志,其丰度可作为预测ICI疗效的新型、精准的生物标志物,优于传统的CD8+ T细胞总量分析。
明确核心免疫抑制性基质细胞:研究首次通过空间蛋白分型证实,肿瘤相关巨噬细胞(TAMs) 和癌相关成纤维细胞(CAFs) 是影响ICI疗效的独立不利因素。这为理解耐药机制提供了明确靶点,即肿瘤微环境中的基质细胞抑制是导致“有细胞但无应答”的核心原因之一。
指导精准联合治疗策略:该发现为克服耐药提供了清晰的联合治疗思路:在增强肿瘤反应性CD8+ T细胞(如靶向CD39/CD103通路)的同时,必须同步靶向TAMs(如CSF-1R抑制剂)或CAFs(如TGF-β抑制剂) 以解除免疫抑制,从而逆转或预防耐药。
临床应用前景:
优化疗效预测模型:在治疗前,通过检测肿瘤组织中CD39+CD103+Ki-67+ CD8+ TILs的密度,结合TAMs与CAFs的丰度,可构建比PD-L1或TMB更精准的ICI疗效预测模型,实现患者的精细化分层。
开发新型联合疗法:为针对TAMs或CAFs的靶向药物与ICI的联合临床试验提供了强力的理论依据和潜在的疗效预测标志物。
动态监测与治疗调整:该空间分型方案可用于治疗过程中的活检样本分析,动态监测关键细胞亚群的变化,为及时调整治疗策略(如加入联合药物)提供依据。
产品应用方案:
阔然生物一站式NGP检测方案,通过纳入CD8、CD39、CD103、Ki-67及巨噬细胞(如CD68/CD163)、成纤维细胞(如α-SMA)等标志物,可实现:
精准鉴定关键T细胞亚群:在单细胞水平精准识别并定量具有预测价值的CD39+CD103+Ki-67+ CD8+ TILs。
全面解析免疫抑制微环境:同步量化免疫抑制性TAMs和CAFs的丰度与空间分布,评估其对T细胞的抑制作用。
空间关系解析:分析上述关键细胞亚群之间的空间邻近关系,揭示细胞间相互作用如何影响疗效。
临床行动建议:
治疗前精准检测:建议对拟接受一线或后线免疫治疗的转移性NSCLC患者,在治疗前活检组织中增加基于多重荧光免疫组化的肿瘤微环境空间分型,重点评估CD39+CD103+Ki-67+ CD8+ TILs、TAMs及CAFs的丰度,用于疗效预测。
设计精准临床试验:鼓励基于上述生物标志物,设计新型联合疗法的临床试验。例如,对TAMs/CAFs高浸润而功能性CD8+ T细胞低丰度的患者,探索ICI联合相应靶向药物的疗效。
耐药后机制探索:对ICI治疗进展后的患者进行再活检,通过相同panel分析微环境变化,明确耐药主因(是功能性T细胞耗竭还是抑制性基质细胞扩增),指导后续治疗方案选择。
总结: 空间单细胞蛋白分型揭示了转移性非小细胞肺癌免疫治疗耐药的核心特征:功能性CD39+CD103+Ki-67+ CD8+ TILs的缺乏与免疫抑制性TAMs/CAFs的富集。这为建立精准的疗效预测模型和设计有效的联合治疗策略提供了双重依据。阔然生物NGP检测方案是实现这一精准分析、推动个体化免疫治疗的关键工具。
十大滚球体育app
Shanghai KR Pharmtech, Co., Ltd.