每日速递:胆囊癌肝转移边界发现决定T细胞命运的“双面”生态位
标题:CXCL9+巨噬细胞与LGALS4+肿瘤细胞“拉锯”,界定胆囊癌肝转移免疫格局
核心临床价值速递:
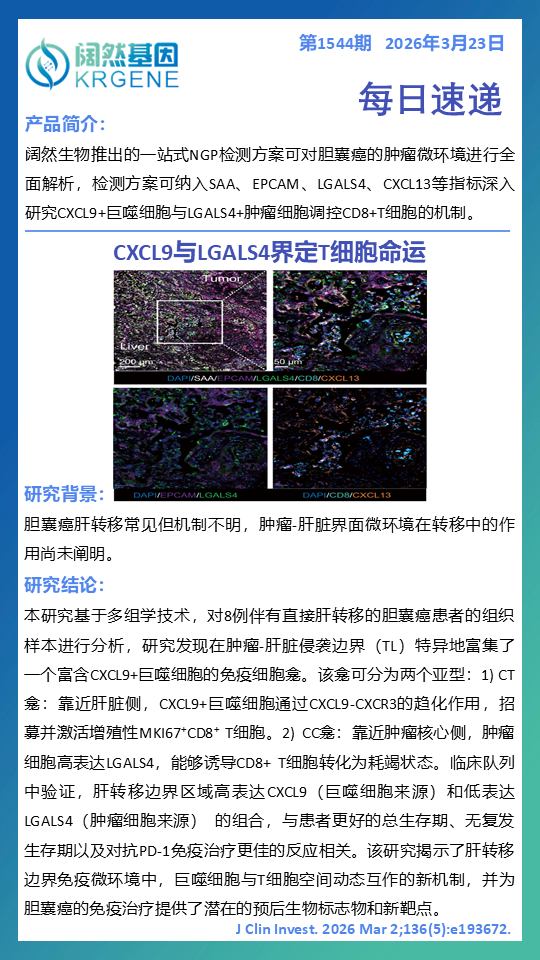
揭示肝转移边界免疫微环境的空间“拉锯战”:本研究首次在胆囊癌肝转移的肿瘤-肝脏侵袭边界,发现了一个结构化的免疫细胞龛,其内部存在决定CD8+ T细胞命运的“空间对决”。靠近肝脏侧为CT龛,其中CXCL9+巨噬细胞通过CXCL9-CXCR3轴招募并激活增殖性CD8+ T细胞;靠近肿瘤侧为CC龛,其中高表达LGALS4的肿瘤细胞则诱导CD8+ T细胞耗竭。
明确关键细胞与分子的临床预后价值:临床队列验证表明,肝转移边界区域高表达CXCL9(巨噬细胞来源) 和低表达LGALS4(肿瘤细胞来源) 的组合特征,是强有力的正面预后标志物,与患者更长的总生存期、无复发生存期以及对PD-1免疫治疗更佳的反应显著相关。
提供全新的预后标志物与联合治疗靶点:该研究不仅为胆囊癌肝转移的预后评估提供了基于空间免疫的精准标志物,更为改善免疫治疗疗效指明了方向:即通过靶向增强“CT龛”(如增强巨噬细胞CXCL9分泌)或抑制“CC龛”(如阻断LGALS4功能),来逆转T细胞耗竭,重塑抗肿瘤免疫。
检测方案与临床落地应用:
技术支撑:阔然生物一站式NGP检测方案,可对胆囊癌原发灶及肝转移灶的肿瘤微环境,特别是侵袭边界,进行高维空间解析。方案精准纳入CXCL9(活化巨噬细胞)、LGALS4(肿瘤细胞)、EPCAM(上皮细胞)、SAA(炎症相关蛋白) 等关键指标,完美适配本研究的验证与临床转化。
核心应用:
空间生态位可视化与分型:在原位精准界定并量化“CT龛”与“CC龛”的空间位置、范围及细胞组成(CXCL9+巨噬细胞 vs. LGALS4+肿瘤细胞),直观展示其与CD8+ T细胞状态的动态关系。
预后评估与治疗预测:对肝转移患者的组织样本(特别是手术切缘或活检样本)进行检测,通过计算“CXCL9高/LGALS4低”评分,实现对患者预后及免疫治疗潜在疗效的精准分层。
机制研究与药物开发:深入解析CXCL9+巨噬细胞的来源与调控机制,以及LGALS4诱导T细胞耗竭的信号通路,为开发靶向该“双面龛”的联合免疫新策略提供关键工具。
临床价值:
将胆囊癌肝转移的研究焦点从细胞组成导向“空间功能生态位”,为理解转移灶免疫逃逸机制提供了革命性的视角。
为临床提供了可操作、可量化的新型免疫预后分层工具,并指出了改善现有免疫治疗疗效的明确干预靶点。
行动建议:
临床病理评估:对于可手术的胆囊癌肝转移患者,建议对切除标本的肿瘤-肝脏边界区域进行NGP空间免疫分析,依据“CXCL9高/LGALS4低”特征进行风险分层,指导术后辅助治疗决策。
治疗策略开发:
探索能够促进肿瘤相关巨噬细胞向CXCL9+表型极化的药物(如某些STING激动剂),或局部给予CXCL9类似物,以增强“CT龛”功能。
开发靶向LGALS4的单克隆抗体或小分子抑制剂,以阻断“CC龛”的免疫抑制作用,并与抗PD-1等免疫检查点抑制剂联用。
研究扩展:在其他易发生肝转移的癌种(如结直肠癌、胃癌)中验证此“双面生态位”模型是否存在,探索其普适性及癌种特异性。
一句话总结:本研究在胆囊癌肝转移边界发现由CXCL9+巨噬细胞和LGALS4+肿瘤细胞主导的、功能相反的“双面”免疫生态位,其平衡状态决定了CD8+T细胞的命运与患者预后,为精准免疫治疗提供了新策略。
十大滚球体育app
Shanghai KR Pharmtech, Co., Ltd.